藤本 学
膠原病
全身性強皮症や皮膚筋炎とその類縁疾患の病態メカニズムについての基礎的研究や臨床的研究を行っており、特に皮膚筋炎では抗TIF1抗体をはじめとする特異的自己抗体におけるサブセット分類に関する先駆的な成果を発表しています。現在、厚生労働省難治性疾患政策研究事業において強皮症研究班の班長、自己免疫疾患研究班において筋炎分科会の分科会長を務めています。
代表論文
- Okiyama N, et al. Distinct histopathologic patterns of finger eruptions in dermatomyositis based on myositis-specific autoantibody profiles. JAMA Dermatol. 155:1080, 2019.
- Fujimoto M, et al. Recent advances in dermatomyositis-specific autoantibodies. Curr Opin Rheumatol. 28:636, 2016.
- Hamaguchi Y, et al. Clinical and immunological predictors of scleroderma renal crisis for Japanese systemic sclerosis patients with anti-RNA polymerase III autoantibodies. Arthritis Rheumatol. 67:1045, 2015.
- Oishi K, et al. A crucial role of L-selectin in C protein-induced experimental polymyositis of mice. Arthritis Rheumatol. 66:1864, 2014.
- Fujimoto M, et al. Autoantibodies to small ubiquitin-like modifier activating enzymes in Japanese patients with dermatomyositis: Comparison with a UK Caucasian cohort. Ann Rheum Dis. 72:151, 2013.
- Le Huu D, et al. FTY720 ameliorates murine Scl-cGVHD by promoting expansion of splenic regulatory cells and inhibiting immune cell infiltration into skin. Arthritis Rheum. 65:1624, 2013.
- Fujimoto M, et al. Myositis-specific anti-155/140 autoantibodies target transcriptional intermediary factor family proteins. Arthritis Rheum. 64:513, 2012.
- Ichimura Y, et al., Anti-NXP2 autoantibodies in adult patients with idiopathic inflammatory myopathies: possible association with malignancy. Ann Rheum Dis. 71:710, 2012.
- Kaji K, et al. Identification of a novel autoantibody reactive with 155- and 140-kDa nuclear proteins in patients with dermatomyositis: an association with malignancy. Rheumatology (Oxford). 46: 25, 2007.
- Saito E, et al. CD19-dependent B lymphocyte signaling thresholds influence skin fibrosis and autoimmunity in the Tight Skin mice. J Clin Invest. 109:1453, 2002.
B細胞
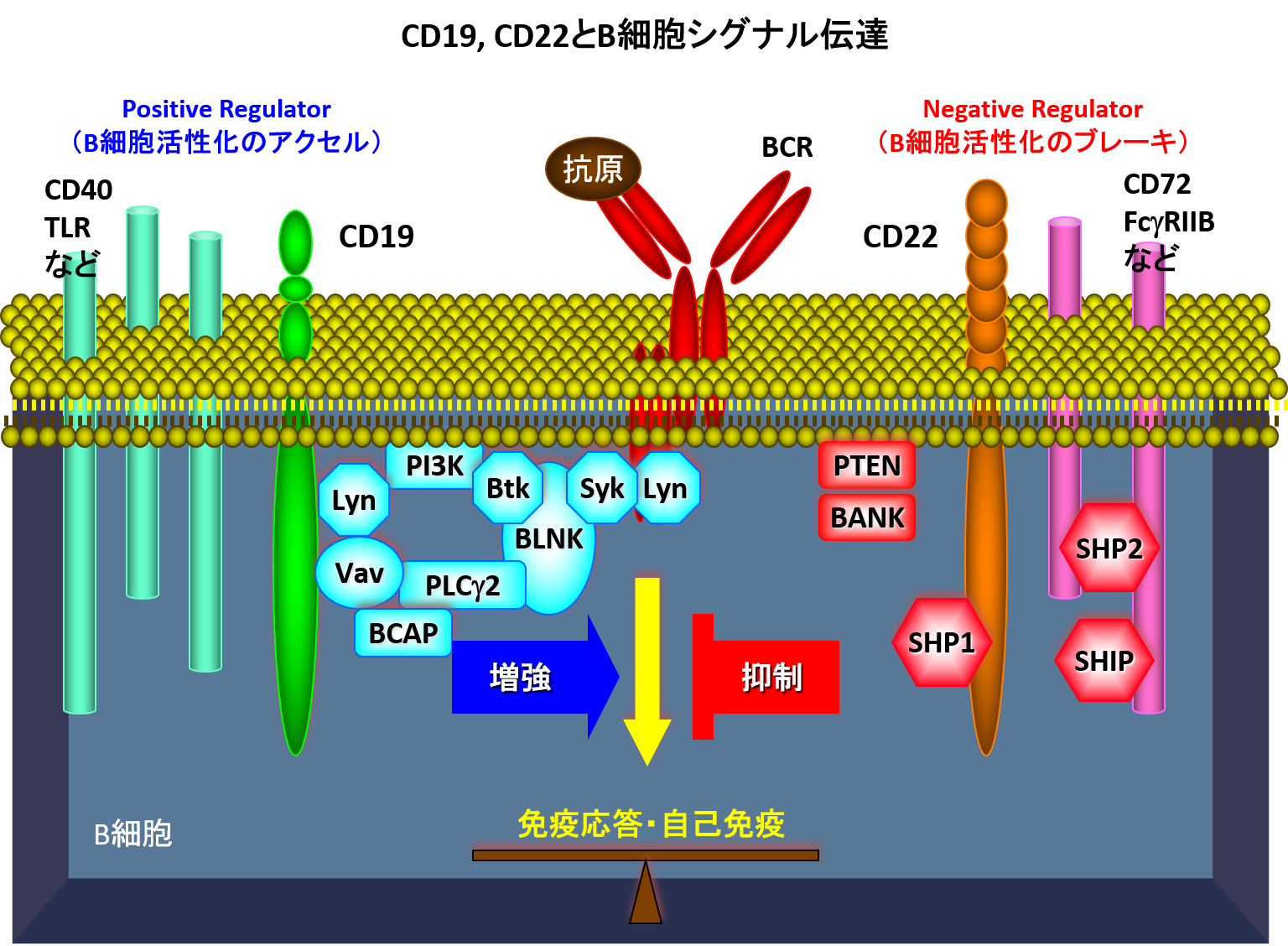
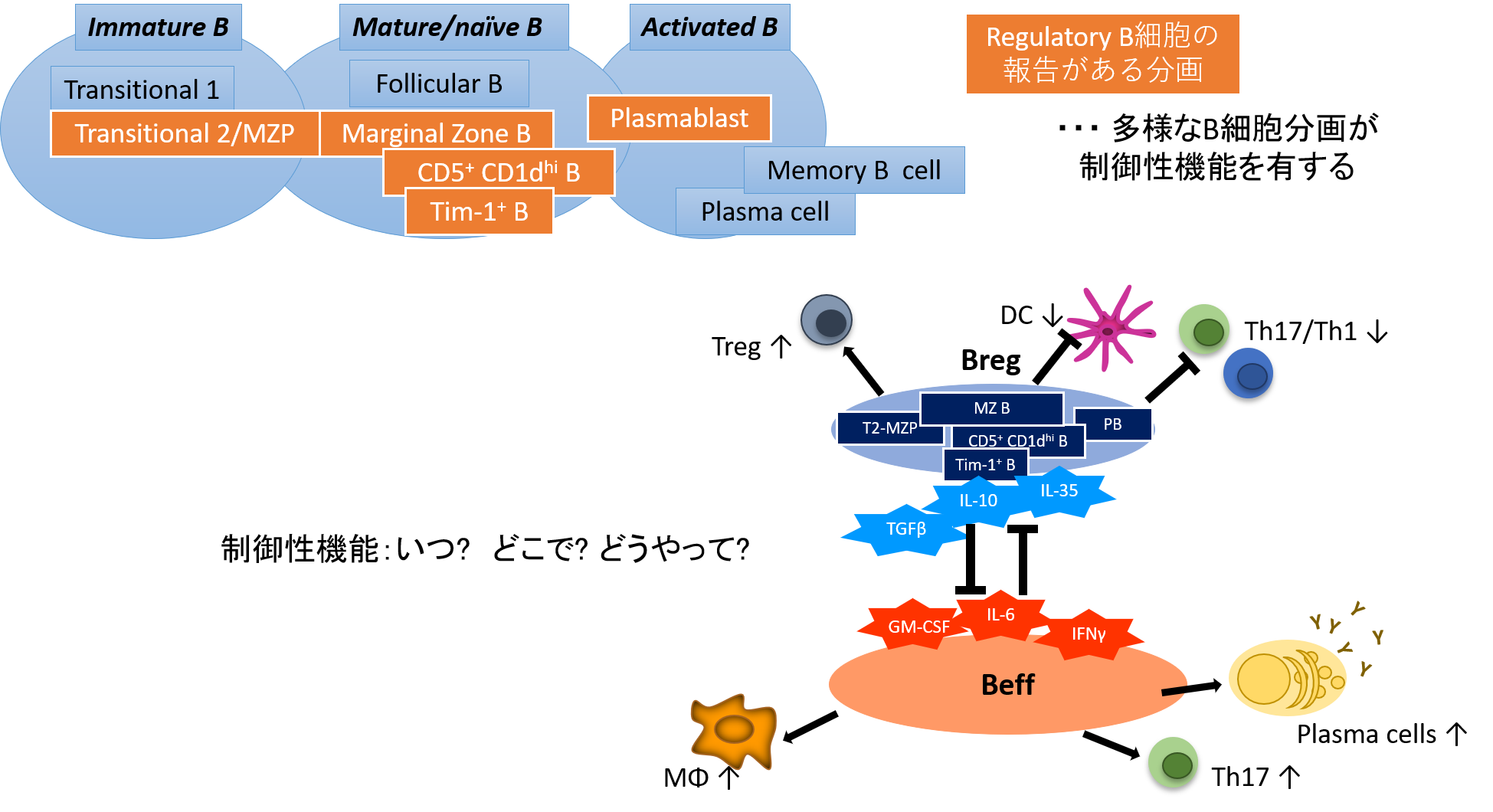
生体の免疫系は、大きく自然免疫と獲得免疫に分けられ、B細胞はこのうち獲得免疫を担うリンパ球とみなされます。B細胞は形質細胞へ分化し抗体産生することから獲得免疫の中でも液性免疫の観点から主に研究が進められていましたが、B細胞にもT細胞との相互作用、サイトカイン産生能など、細胞自体のエフェクター機能があることが明らかになっています。私達はB細胞の膜表面シグナル伝達分子CD19, CD22を中心に、B細胞におけるシグナル伝達メカニズムと自己免疫疾患の関連について研究を行ってきました。また、免疫反応を抑制する新しいB細胞サブセットであるregulatory B細胞(Breg)の皮膚免疫疾患における役割についても先駆的な成果をあげています。
皮膚に分布しないとされるB細胞が、樹状細胞、T細胞などとの相互作用を通して皮膚疾患の制御に関わるという考え方は、全身疾患の表れとして捉えられるべき皮膚疾患の性質に合致します。皮膚疾患の背景にある免疫応答の過程をB細胞の観点から理解し、皮膚疾患の病態を明らかにしていきたいと考えています。
代表論文
- Matsushita T, et al. A novel splenic B1 regulatory cell subset suppresses an allergic disease via PI3K-Akt pathway activation. J Allergy Clin Immunol. 138:1170, 2016
- Le Huu D, Matsushita T, Jin G, et al. Donor-derived regulatory B cells are important for suppression of murine sclerodermatous chronic graft-versus-host disease. Blood. 121:3274-3274, 2013.
- Jin G, Hamaguchi Y, Matsushita T, et al. BLNK expression contributes to controlling allergic and autoimmune diseases by mediating IL-10 production in regulatory B cells. J Allergy Clin Immunol. 31:1674-1674, 2013.
- Watanabe R, Ishiura N, Nakashima H, et al. Regulatory B cells (B10 cells) have a suppressive role in murine lupus: CD19 and B10 cell deficiency exacerbates systemic autoimmunity. J Immunol. 184:4801, 2010.
- Matsushita T, et al. Regulatory B cells inhibit EAE initiation while other B cells promote disease progression. J Clin Invest. 118:3420, 2008.
- Yanaba K, et al. A regulatory B cell subset with a unique CD1dhighCD5+ phenotype controls T cell-dependent inflammatory responses. Immunity. 28:639, 2008.
- Poe JC, et al. CD22 regulates B lymphocyte function in vivo through both ligand-dependent and -independent mechanisms. Nat Immunol. 2004;5:1078, 2004.
- Yazawa N, Fujimoto M, Sato S, et al. CD19 regulates innate immunity by toll-like receptor RP105 signaling in B lymphocytes. Blood. 102:1374, 2003.
- Fujimoto M, Fujimoto Y, Poe JC, et al. CD19 regulates Src-family protein tyrosine kinase activation in B lymphocytes through processive amplification. Immunity. 13:47, 2000.
- Fujimoto M, Bradney A, Poe JC, et al. Modulation of B lymphocyte antigen receptor signal transduction by a CD19/CD22 regulatory loop. Immunity. 11:191, 1999.
渡邉 玲
皮膚resident memory T細胞
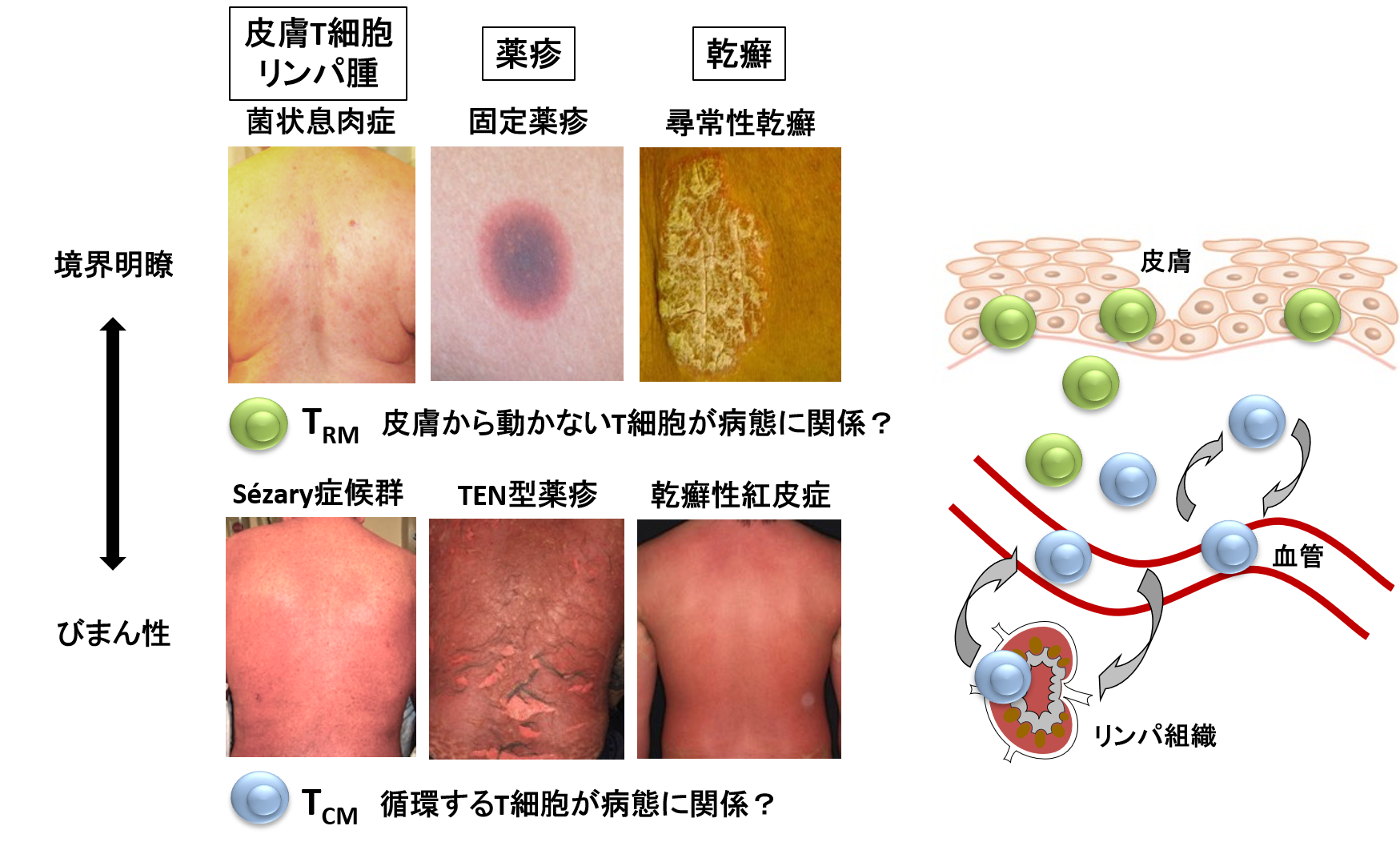
T細胞は従来主に循環中の分画から機能の研究がなされてきましたが、末梢組織に一旦移行した後、再循環せず組織にとどまり続けるT細胞分画の存在が知られるようになりました。この細胞分画はresident memory T細胞と名付けられ、循環中T細胞との機能の相違について研究が進められています。人体で細胞の動きや機能を経時的に追いかけることは非常に難しいですが、健常人のバリア組織の免疫機構、臓器特異的自己免疫疾患への関与などの観点から研究が進められています。
私達は、皮膚resident memory T細胞が様々な皮膚疾患の病態にどのように影響しているかを解明し、T細胞機能の正常化を軸とした疾患治療薬を開発することを目指しています。また健常人皮膚においても、resident memory T細胞機能の加齢変化を探索し、T細胞機能の観点から皮膚バリア機能保持機構の解明を目指しています。
代表論文
- Koguchi-Yoshioka H, Watanabe R, Fujisawa Y, et al. Skin resident memory T-cell population is not constructed effectively in systemic sclerosis. Br J Dermatol. 180:219-220, 2019.
- Vo S, Watanabe R, Koguchi-Yoshioka H, et al. CD8 resident memory T cells with IL-17A-producing potential are accumulated in disease-naïve non-lesional sites of psoriasis possibly in correlation with disease duration. Br J Dermatol. 181:410-412,2019.
- Nakamura Y, Watanabe R, Zhenjie Z, et al. CD103 negative memory T cells may play important roles in making regulatory T-cell-enriched environments in skin tumours. J Eur Acad Dermatol Venereol. 2019 Epub ahead of print.
- Watanabe R. Protective and pathogenic roles of resident memory T cells in human skin disorders. J Dermatol Sci. 95:2-7,2019 (review article).
- Kirsch IR*, Watanabe R*, O’Malley JT, et al. TCR sequencing facilitates diagnosis and identifies mature T cells as the cell of origin in CTCL. Sci Transl Med. Vol.7:308ra158, 2015. *co-first authors
- Watanabe R, Gehad A, Yang C, et al. Human skin is protected by four functionally and phenotypically discrete populations of resident and recirculating memory T cells. Sci Transl Med. 7:279ra39, 2015.
松岡 悠美
アトピー性皮膚炎などの慢性炎症性皮膚疾患における常在細菌叢・炎症を引き起こす病原細菌の関連についての研究
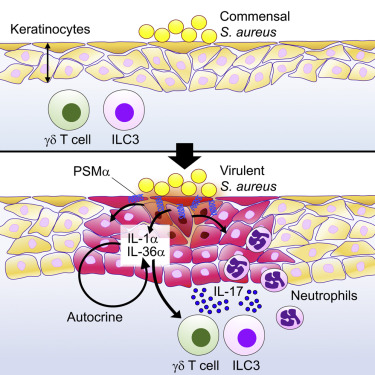
アトピー性皮膚炎などの慢性炎症性皮膚疾患における常在細菌叢と、炎症を引き起こす病原細菌の関連について研究を行っています。細菌には、クオラムセンシングという自身の生息密度を感知するシステムが備わっており、皮膚における細菌叢の乱れ(Dysbiosis)が起こると、病原菌のクオラムセンシングが発動します。すると、菌からの毒素の産生が引き起こされ、皮膚炎が起こります。これらのメカニズムと病態への関与を明らかにし、新規治療ターゲットの探索などの足がかりを構築するため、マウスモデルを用いた解析や、ヒトから単離された菌の遺伝子およびその発現を解析するなどの様々なアプローチを行っております。
代表論文
- Nakamura Y, Takahashi H, Takaya A, Inoue Y, Katayama Y, Kusuya Y, Shoji T, Takada S, Nakagawa S, Oguma R, Saito N, Ozawa N, Nakano T, Yamaide F, Dissanayake E, Suzuki S, Villaruz A, Varadarajan S, Matsumoto M, Kobayashi T, Kono M, Sato Y, Akiyama M, Otto M, Matsue H, Núñez G, Shimojo N. Staphylococcus Agr virulence is critical for epidermal colonization and associates with atopic dermatitis development. Sci Transl Med. 2020 Jul 8;12(551): eaay4068.
- Baldry M, Nakamura Y, Nakagawa S, Frees D, Matsue H, Núñez G, Ingmer H. Application of an agr-specific anti-virulence Compound as Therapy for Staphylococcus Aureus-induced Inflammatory Skin Disease. J Infect Dis. 2018; May 4. doi: 10.1093/infdis/jiy259.
- Nakagawa S, Matsumoto M, Katayama Y, Oguma R, Wakabayashi S, Nygaard T, Saijo S, Inohara N, Otto M, Matsue H, Núñez G, Nakamura Y. Staphylococcus aureus Virulent PSMα Peptides Induce Keratinocyte Alarmin Release to Orchestrate IL-17-Dependent Skin Inflammation. Cell Host Microbe. 2017; 22(5):667-677
- Nakamura Y, Oscherwitz J, Cease KB, Chan SM, Muñoz-Planillo R, Hasegawa M, Villaruz AE, Cheung GY, McGavin MJ, Travers JB, Otto M, Inohara N, Núñez G. Staphylococcus δ-toxin promotes allergic skin disease by inducing mast cell degranulation. Nature. 2013; Nov 21;503(7476):397-401.
- Franchi L, Kamada N, Nakamura Y, Burberry A, Kuffa P, Suzuki S, Shaw MH, Kim YG, Núñez G. NLRC4-driven production of IL-1β discriminates between pathogenic and commensal bacteria and promotes host intestinal defense. Nat Immunol. 2012 May;13(5):449-56.
植田 郁子
膠原病および膠原病類縁疾患の病態にかかわるT細胞サブセットの探索
膠原病は原因不明の難治性疾患ですが、その病態にB細胞やT細胞などが関わっていると考えられています。血液中の細胞の表面マーカーを種々の抗体で染色することにより各種サブセットに分類し、その数や頻度の異常、活性化の有無、機能異常の有無、皮膚病変への関連などを調べ、病態の解明や病状の把握に結びつくかを検討しています。
荒瀬規子
細胞内ミスフォールド蛋白/MHCクラスII複合体と自己免疫疾患発症機構についての研究
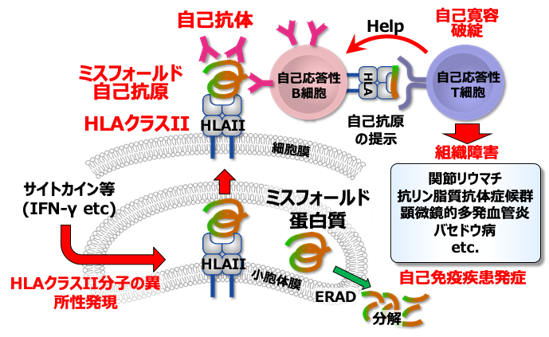 細胞内ミスフォールドタンパク質はMHCクラスIIと会合し細胞表面に発現しました。 さらにミスフォールド蛋白/MHCクラスII複合体は自己免疫疾患で自己抗体の標的分子となっていました。 自己抗体産生や自己免疫疾患発症の分子機構を明らかにしていけたらと考えています。 |
|
NK細胞等自然免疫細胞が発現するレセプター分子の研究
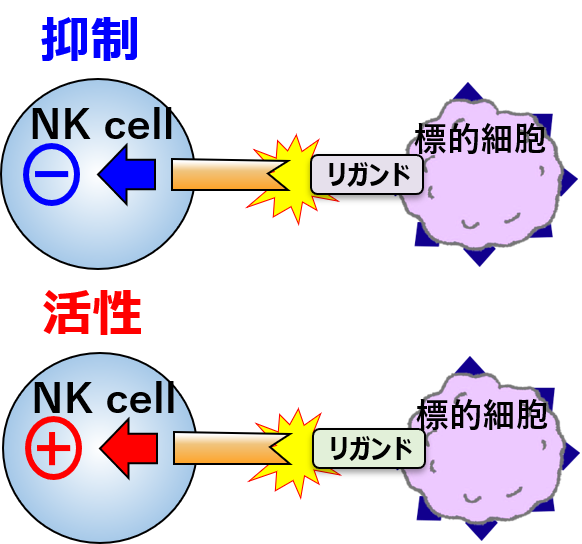 病原体などに対する生体防御には、獲得免疫以外に自然免疫も働きます。 一部の病原体は自然免疫細胞の抑制化受容体に対するリガンドを発現し免疫から逃れます。 一方免疫細胞は抑制化受容体から進化した活性化受容体で生体を防御してきました。 これら自然免疫レセプターの種々の皮膚疾患における役割を解析しています。 Arase N, et al. Int Immunol. 17:1227-1237, 2005. |
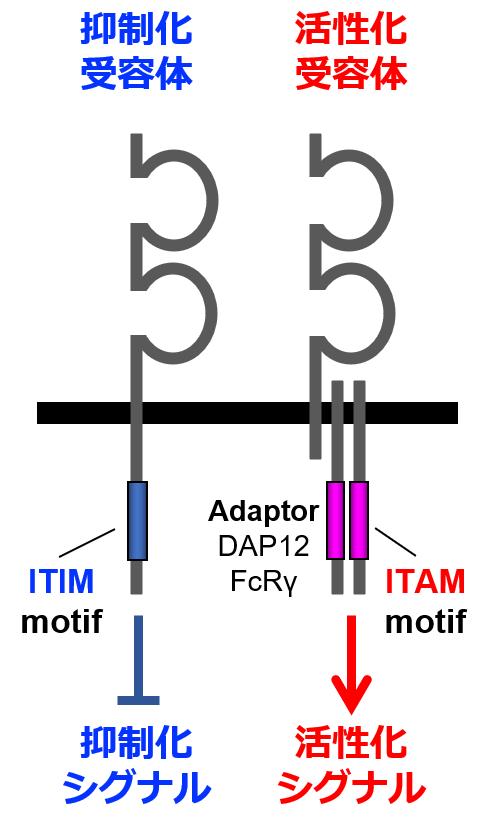 |
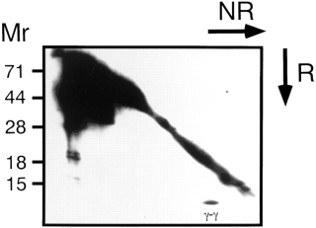 NK細胞活性化レセプターがITAMモチーフのアダプター分子・FcRγと会合する事を初めて明らかにしました。 自然免疫に関係する各種レセプターのリガンドのクローニングにも成功してきました。 |
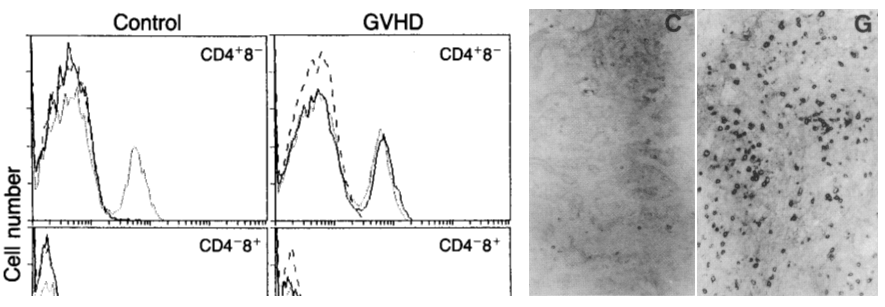
皮膚のgraft versus host disease (GVHD)に関する研究
難治性皮膚疾患における遺伝子解析研究
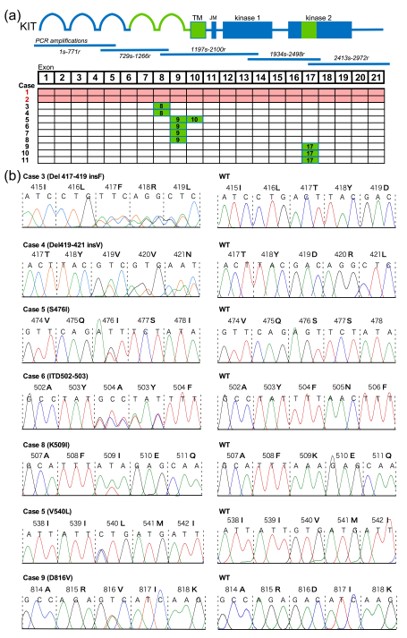 日本人肥満細胞増多症のc-KIT 変異パターンを決定しました。 Arase N, et al. J Dermatol. 47:426-429, 2020. |
皮膚科の診療では教科書に載っていないような珍しい症状を持つ患者さんに出会うことがあります。
Symmetrical acral keratodermaにfilaggrin |
代表論文
- Miki Kume, Noriko Arase, Naokko Okiyama, Hanako Koguchi-Yoshioka, Tomomi Tada, Hiroko Saruban, Manabu Fujimoto
Unilateral heliotrope rash: a warning sign for anti-melanoma differentiation-
associated gene 5 antibody-positive dermatomyositis
Rheumatology. in press. - Arase N, Tanemura A, Jin H, Nishioka M, Aoyama Y, Oiso N, Matsunaga K, Suzuki T, Nishigori C, Kawamura T, Shimizu T, Ito A, Fukai K, Abe Y, Yang L, Tsuruta D, Takeoka K, Iwatani Y, Hidaka Y, Nishida M, Yamauchi-Takihara K, Arase H, Fujimoto M, Katayama I.
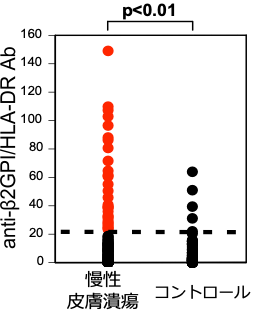
Autoantibodies detected in patients with vitiligo vulgaris but not in those with rhododendrol-induced leukoderma. J Dermatol Sci. 95:80-83, 2019. - Arase N, Arase H.
Cellular misfolded proteins rescued from degradation by MHC class II molecules are possible targets for autoimmune diseases.
J Biochem. 158:367-372, 2015. - Jin H, Arase N, Hirayasu K, Kohyama M, Suenaga T, Saito F, Tanimura K, Matsuoka S, Ebina K, Shi K, Toyama-Sorimachi N, Yasuda S, Horita T, Hiwa R, Takasugi K, Ohmura K, Yoshikawa H, Saito T, Atsumi T, Sasazuki T, Katayama I, Lanier LL, Arase H.
Autoantibodies to IgG/HLA class II complexes are associated with rheumatoid arthritis susceptibility.
Proc Natl Acad Sci U S A. 111:3787-3792, 2014. - Jiang Y*, Arase N*, Kohyama M, Hirayasu K, Suenaga T, Jin H, Matsumoto M, Shida K, Lanier LL, Saito T, Arase H. (*co-first authors)
Transport of misfolded endoplasmic reticulum proteins to the cell surface by MHC class II molecules
Int Immunol. 25:235-246. 2013.
金田 眞理
結節性硬化症の病態解明
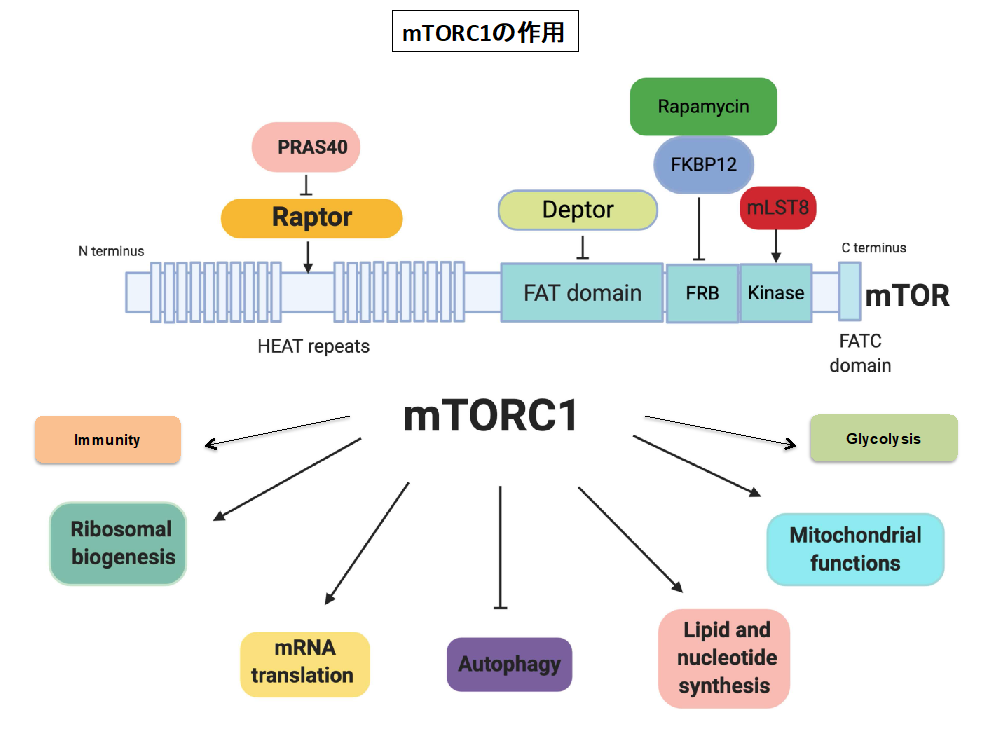
これらmTORC1の機序解明と同時に通常は皮膚を通して皮下の組織に入りにくいmTORC1阻害剤シロリムスを、特殊な基剤を用いて、表皮を通して皮下の腫瘍組織に到達させる事に成功し、結節性硬化症の皮膚病変に特化した安全性の高い治療薬の開発を行ってきた。本外用薬は本邦では市販され、現在は海外承認を待っている。
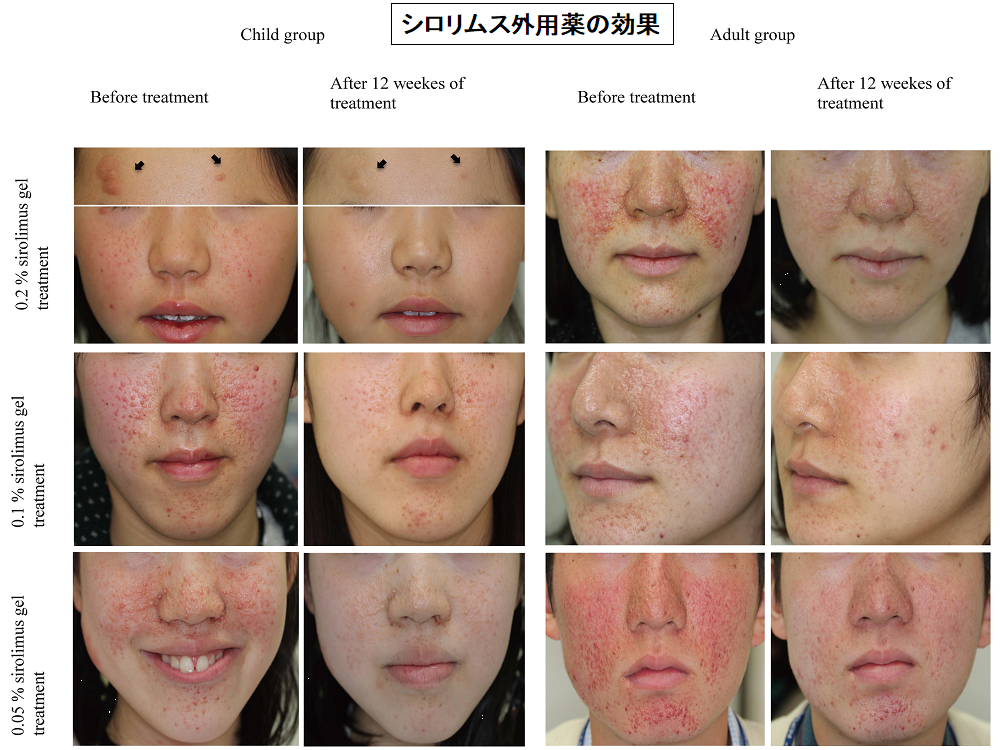
参考文献
- Dermatology and Therapy 2020 May 8. Safety and Efficacy of the Sirolimus Gel for TSC Patients With Facial Skin Lesions in a Long-Term, Open-Label, Extension, Uncontrolled Clinical Trial.
- JAMA Dermatol. 2018 1;154(7):781-788 . Sirolimus Gel Treatment vs Placebo for Facial Angiofibromas in Patients With Tuberous Sclerosis Complex: A Randomized Clinical Trial.
- JAMA Dermatol. 2017 Jan 1;153(1):39-48. Efficacy and Safety of Topical Sirolimus Therapy for Facial Angiofibromas in the Tuberous Sclerosis Complex A Randomized Clinical Trial.
- PLOS ONE 2020 Jan 24;15(1):e0228204. Epilepsy in a melanocyte-lineage mTOR hyperactivation mouse model: A novel epilepsy model.
- J Invest Dermatol. 2018 Mar;138(3):669-678. Uncoupling of ER/mitochondrial oxidative stress in mTORC1 hyperactivation-associated skin hypopigmentation.
- J Dermatol Sci. 2018 Feb;89(2):155-164. Dysregulation of autophagy in melanocytes contributes to hypopigmented macules in tuberous sclerosis complex.
清原 英司
皮膚微小環境における皮膚リンパ腫の動態解析と新規治療探索
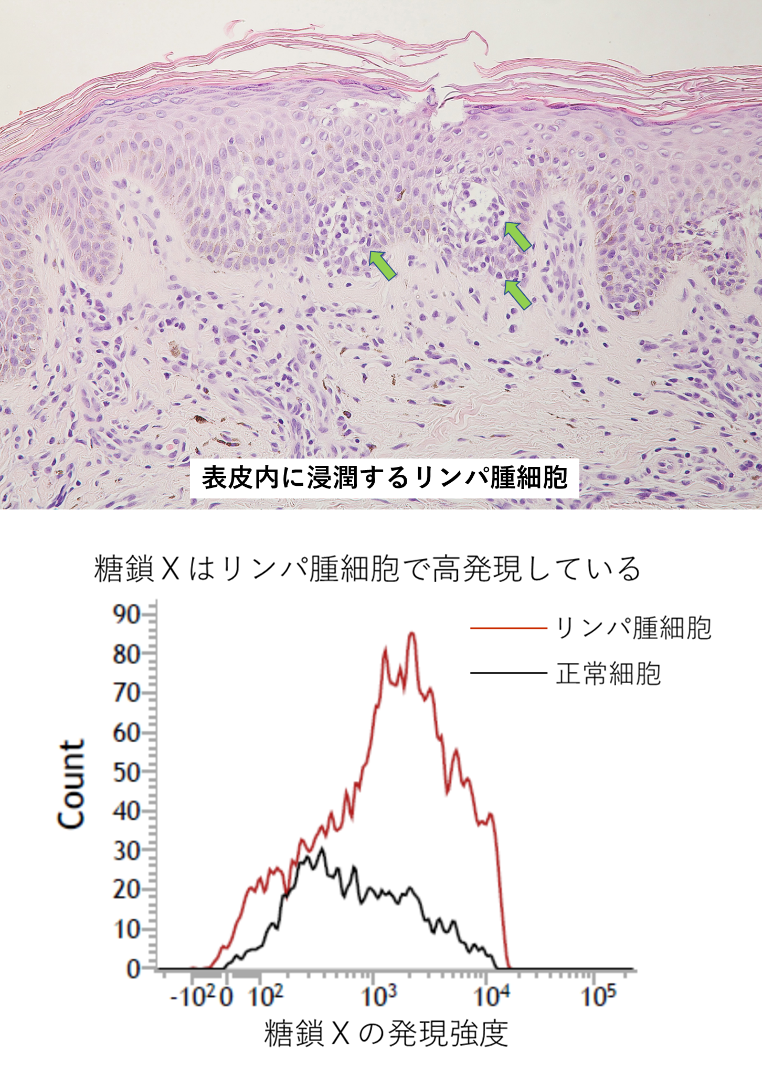
しかし皮膚の免疫環境は複雑であり、定常状態にあるリンパ球からリンパ腫への発症機序や抗腫瘍免疫のメカニズムは不明な点が多々あります。大阪大学皮膚科では以前より多数の症例を専門外来にて治療しており、その経験に基づいて腫瘍微小環境が固形腫瘍と比較してどのように異なるのかを解析し、新規治療ターゲットの探索などを行っています。
現在、糖鎖と腫瘍免疫の関係をはじめとして研究分野を広げており、最終的に研究成果を患者へ還元できるようにしたいと思います。
種村 篤
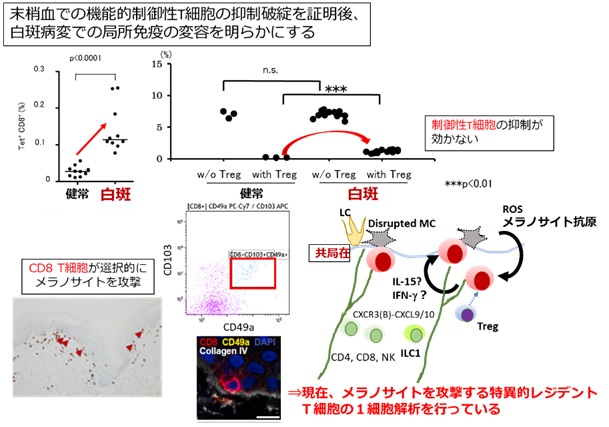
白斑でのメラノサイトに対する自己免疫応答調節機構の解明
我々は、白斑でのメラノサイトに対する自己免疫応答調節機構の解明を研究テーマとして、
「なぜ、白斑は強い炎症を伴わず生じるのか?」
「なぜ、左右対称性に白斑が分布するのか?」
「なぜ、色素の再脱失を生じるのか?」
といった臨床に直結する疑問を明らかにしたいと思っています。少しでも興味のある方、ご連絡お待ちしています。
研究メンバー:種村 篤、横井一範(大学院生)
参考文献
- Itoi S, Tanemura A, Kotobuki Y, et al. Coexistence of Langerhans cells activation and immune cells infiltration in progressive nonsegmental vitiligo. J Dermatol Sci 2014:73:83-85.
- Tanemura A, Yang L, Katayama I. Dysregulation of circular antigen-specific T cells anergy in autoimmune vitiligo. JCDSA 2018;8:133-139.
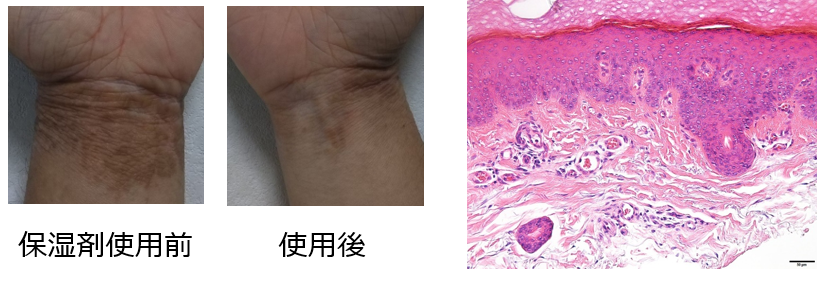
- Katsuda K, Tanemura A, Takafuji M, et al. A rare case of segmental vitiligo in wich lesional enlargement occurred after suction blister transplantation. J Dermatol 2020. Epub ahead of print.